Una máquina térmica es un sistema conectado a una fuente de calor a temperatura ![]() , que es capaz de hacer
un trabajo W
y liberar calor a una fuente de calor a temperatura
, que es capaz de hacer
un trabajo W
y liberar calor a una fuente de calor a temperatura ![]() con
con ![]() .
.
Se defina la eficiencia de dicha máquina por:
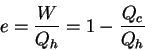
Según esta ecuación, una máquina térmica tiene 100% de eficiencia sólo si ![]() . La experiencia
muestra que esto es imposible. Esto constituye la forma Kelvin-Planck de la
Segunda Ley de la Termodinámica:
Es imposible hacer una máquina térmica que, operando en un ciclo, no produzca otro efecto que la absorción
de energía de un depósito y la realización de una cantidad de trabajo equivalente.
. La experiencia
muestra que esto es imposible. Esto constituye la forma Kelvin-Planck de la
Segunda Ley de la Termodinámica:
Es imposible hacer una máquina térmica que, operando en un ciclo, no produzca otro efecto que la absorción
de energía de un depósito y la realización de una cantidad de trabajo equivalente.
Tal máquina, si existiera, sería una máquina perfecta.